前回はんだ付けについて書きましたので、その続きでフラックスの酸化膜除去効果について調べました。
はんだ付けをする際には、母材の銅表面に生じる酸化膜を除去しないときれいにはんだ付けすることができません。
酸化膜を除去するために、フラックス(ロジンと呼ばれる松脂の不揮発性成分と有機酸塩やアミンなどの活性剤から成るものが代表的)が還元剤として用いられます。
ロジンの代表は下のような化合物で、カルボキシ基を持ちます。
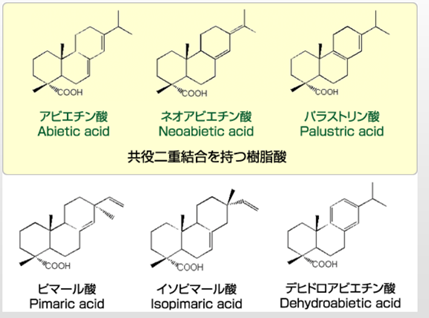
電極によく使われる銅を例にみてみますと、
銅の酸化膜を還元する化学反応式はRを用いて以下のように表されます。
CuO+2RCOOH→Cu(RCOO)2+H2O
ここで、アルデヒド基の還元性の話を思い出して混乱してしまいました。
岡野の化学で学習したのは、アルデヒドは自身が参加してカルボン酸になるので還元剤として働く、アルデヒドはフェーリング反応を示すがカルボン酸は示さない(ギ酸は例外)というものでした。
ここでRはHに限定されませんので、ギ酸以外のカルボン酸も還元剤として働いてCuOから酸素を取り除くことができるということになります。
上の反応式でもフラックス自身はHを失って酸化されていますので、還元剤として働いたと言えます。なぜでしょうか。
考えついた説明としては、
まず酸化還元は相対的な概念で、相手によって酸化剤として働くか還元剤として働くかが変わるため、カルボン酸はフェーリング反応などでは還元剤として働かなかったが、CuOが相手だと還元剤として働くというものです。
また生成されたCu(RCOO)2が安定しているということも言えると思います。
カルボン酸は二量体を作りやすいという特徴があります。
下図のように水素結合でカルボキシ基同士が引き付け合います。
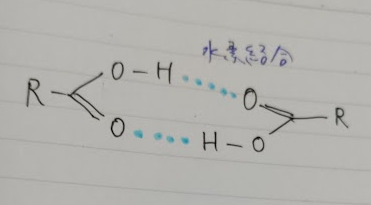
この構造を書いてじっと見ていたところピンときました。キレート効果です。
このように4つのO原子が銅イオンを安定化していると考えました。
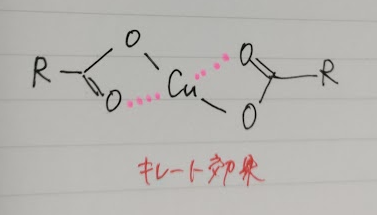
そこでこれを裏付けるような構造式が出ていないかと探したところ、
Google Patentsで以下の図が出ているものを見つけました。
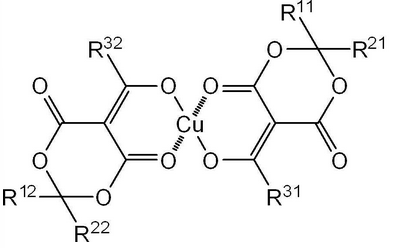
しかしよく読んでみると、この特許は「有機銅錯体を用いて銅酸化物薄膜を形成する方法」に関するものでした。ということは、フラックスを使って銅酸化膜を取り除いても、今度は錯体がまた新しい膜を形成してしまうということになります。
調べてみると、はんだ付けが済んでフラックスの役目が終わった後は、フラックス残渣を除去する洗浄工程があるということでした。
またロジンの誘導体にはインクや接着剤など色々な用途があり、パインケミカルという一つの領域になっているということも分かりましたので、こちらも何かの時にフックがかかるように、用途を確認します。
6/18(火)学習時間:9.75H
・岡野の化学(128)
・フラックスの効果について
・リフロー法について
課題)
・ロジンの用途について
・特許明細書を読むにあたっての背景知識の補充の続き
(SOI素子、オーミックコンタクト、濡れ性の評価方法、SEMの原理)
その他
・0815 溶液・溶質・溶媒
・4659 トライアル合格は出口ではない







コメントを残す